FAQ zur Klinischen Prüfung mit Medizinprodukten
Viele Hersteller werden vor eine große Herausforderung gestellt, wenn sich im Rahmen der klinischen Bewertung über den Literaturweg herausstellt, dass nicht ausreichend klinische Daten zur Verfügung stehen, um die Konformität mit den Grundlegenden Anforderungen (EU RL 93/42EWG, Anhang I) zu zeigen und somit eine klinische Prüfung erforderlich wird.
Häufig besteht eine große Unsicherheit bezüglich der Regularien für klinische Prüfungen mit Medizinprodukten sowie Unklarheit darüber, für welche Art von Medizinproduktestudien welche Art von Genehmigungen und Voten vorliegen müssen.
Um Ihnen den Einstieg in die klinische Prüfung mit Medizinprodukten zu erleichtern, haben wir für Sie im Folgenden einige wichtige Fragen und Antworten zu diesem Thema zusammengestellt.
Klinische Prüfungen von Medizinprodukten im Sinne des Medizinproduktegesetzes dienen der Erhebung von klinischen Daten, die zur Durchführung einer klinischen Bewertung erforderlich sind.
Eine Definition der klinischen Prüfung ist weder in der RL 93/42/EWG, noch im Medizinproduktegesetz und der Verordnung über die klinische Prüfung mit Medizinprodukten (MPKPV) zu finden.
Gemäß der DIN EN ISO 14155 ist die klinische Prüfung definiert als eine „systematische Prüfung an einer oder mehreren Versuchsperson(en), die vorgenommen wird, um die Sicherheit oder Leistungsfähigkeit eines Medizinprodukts zu bewerten“1.
Die klinische Prüfung ist in der Regel immer dann erforderlich, wenn sich im Rahmen der klinischen Bewertung herausstellt, dass nicht ausreichend klinische Daten aus der Literatur zur Verfügung stehen, um die Konformität mit den Grundlegenden Anforderungen (Anhang I RL 93/42/EWG) für das betreffende Medizinprodukt nachzuweisen.
Über die klinische Prüfung werden die noch fehlenden klinischen Daten für das betreffende Medizinprodukt erhoben, die zum Nachweis der Erfüllung der Grundlegenden Anforderungen notwendig sind.
Die klinische Prüfung verfolgt somit die gleichen Ziele wie die klinische Bewertung, nämlich
- zu bestätigen, dass die Leistungen des Produkts bei normalen Einsatzbedingungen den vom Hersteller gemachten Leistungsangaben entsprechen, und
- bei normalen Einsatzbedingungen auftretende unerwünschte Nebenwirkungen des Produkt zu ermitteln und zu beurteilen, ob diese unter Berücksichtigung der vorgegebenen Leistungen ein Risiko für den Patienten beinhalten.
Im Medizinproduktegesetz ist die Erforderlichkeit der klinischen Prüfung allerdings nicht explizit geregelt.
Der Gesetzgeber verweist uns hier auf den Anhang X, Punkt 1.1.a der RL 93/42/EWG, welcher ausweist, dass klinische Prüfungen bei Produkten der Klasse III und implantierbaren Produkten durchzuführen sind.
Durch den Zusatz „es sei denn, die Verwendung bereits bestehender klinischer Daten ist ausreichend gerechtfertigt“2, besteht auch für diese Produkte nicht zwingend eine Verpflichtung eine klinische Prüfung durchzuführen.
Es gibt zahlreiche Regularien/Vorschriften, die sehr konkrete Vorgaben machen, wie eine klinische Prüfung mit einem Medizinprodukt durchzuführen ist. Dazu zählen:
- Richtlinie 93/42/EWG über Medizinprodukte
- Medizinproduktegesetz (MPG)
- Verordnung über die klinische Prüfung von Medizinprodukten (MPKPV)
- Medizinprodukte-Sicherheitsplanverordnung (MPSV)
- Verordnung über das datenbankgestützte Informationssystem über Medizinprodukte (DIMDIV)
- DIN EN ISO 14155 Klinische Prüfung von Medizinprodukten an Menschen
- Deklaration von Helsinki
In der EU-Richtlinie 93/42/EWG (vom 14.06.1993, zuletzt geändert über die Änderungs-Richtlinie 2007/47/EG, welche am 21.03.2010 in Kraft trat) wird der Rechtsrahmen über die allgemeinen Anforderungen an die Durchführung der klinischen Prüfung von Medizinprodukten im Artikel 15 mit den Anhängen VIII und X definiert.
In deutsches Recht umgesetzt sind diese Anforderungen aus der EU-Richtlinie 93/42/EWG im Medizinproduktegesetz (MPG) in den §§20 – 24. Durch die Novellierung des MPG über das Gesetz zur Änderung medizinprodukterechtlicher Vorschriften (4. MPG Novelle, in Kraft getreten am 21.03.2010), wurden die grundsätzlichen und formalen Anforderungen an die klinische Prüfung mit Medizinprodukten noch einmal verschärft und an das Arzneimittelgesetz (AMG) angeglichen. Die Paragrafen §§ 20 bis 22 entsprechen im Wesentlichen den §§ 40-42 AMG.
Artikel 15 RL93/42/EWG
(1) Bei Produkten, die für klinische Prüfungen bestimmt sind, wendet der Hersteller oder der in der Gemeinschaft niedergelassene Bevollmächtigte das in Anhang VIII genannte Verfahren an und meldet dies anhand der in Anhang VIII Abschnitt 2.2 genannten Erklärung den zuständigen Behörden der Mitgliedstaaten, in denen die Prüfungen durchgeführt werden sollen.
(2) Bei Produkten der Klasse III sowie bei implantierbaren und zur langzeitigen Anwendung bestimmten invasiven Produkten der Klasse IIa oder IIb kann der Hersteller mit den betreffenden klinischen Prüfungen nach Ablauf einer Frist von 60 Tagen nach dieser Mitteilung beginnen, es sei denn, die zuständigen Behörden haben ihm innerhalb dieser Frist eine auf Gründe der öffentlichen Gesundheit oder der öffentlichen Ordnung gestützte gegenteilige Entscheidung mitgeteilt.
Die Mitgliedstaaten können die Hersteller jedoch ermächtigen, vor Ablauf der Frist von 60 Tagen mit den klinischen Prüfungen zu beginnen, sofern die betreffende Ethik-Kommission eine befürwortende Stellungnahme zu dem entsprechenden Prüfungsprogramm einschließlich ihrer Überprüfung des klinischen Prüfplans abgegeben hat.
(3) Bei anderen als den in Absatz 2 genannten Produkten können die Mitgliedstaaten die Hersteller ermächtigen, sofort nach der Mitteilung mit der klinischen Prüfung zu beginnen, sofern die zuständige Ethikkommission eine befürwortende Stellungnahme zu dem entsprechenden Prüfungsprogramm, einschließlich ihrer Überprüfung des klinischen Prüfplans abgegeben hat.
(4) Die Ermächtigung nach Absatz 2 Unterabsatz 2 bzw. nach Absatz 3 kann von einer Genehmigung durch die zuständige Behörde abhängig gemacht werden.
(5) Die klinischen Prüfungen müssen gemäß Anhang X durchgeführt werden. Die Maßnahmen zur Änderung nicht wesentlicher Bestimmungen dieser Richtlinie durch Ergänzung, die die Bestimmungen für klinische Prüfungen in Anhang X betreffen, werden nach dem in Artikel 7 Absatz 3 genannten Regelungsverfahren mit Kontrolle erlassen.
(6) Die Mitgliedstaaten ergreifen, falls erforderlich, die geeigneten Maßnahmen zur Sicherung der öffentlichen Gesundheit und öffentlichen Ordnung. Wird eine klinische Prüfung von einem Mitgliedstaat abgelehnt oder ausgesetzt, so unterrichtet dieser Mitgliedstaat alle anderen Mitgliedstaaten und die Kommission von seiner Entscheidung und deren Gründen. Hat ein Mitgliedstaat eine wesentliche Änderung oder vorübergehende Unterbrechung einer klinischen Prüfung angeordnet, so unterrichtet dieser Mitgliedstaat die betroffenen anderen Mitgliedstaaten von seinen Maßnahmen und deren Gründen.
(7) Der Hersteller oder sein Bevollmächtigter unterrichtet die zuständigen Behörden des betroffenen Mitgliedstaats über den Abschluss der klinischen Prüfungen mit einer entsprechenden Begründung im Fall einer vorzeitigen Beendigung. Im Fall der vorzeitigen Beendigung der klinischen Prüfungen aus Sicherheitsgründen ist diese Mitteilung allen Mitgliedstaaten und der Kommission zu übermitteln. Der Hersteller oder sein Bevollmächtigter hält den in Anhang X Abschnitt 2.3.7 genannten Bericht den zuständigen Behörden zur Verfügung.
(8) Die Bestimmungen der Absätze 1 und 2 gelten nicht, wenn die klinischen Prüfungen mit Produkten durchgeführt werden, die gemäß Artikel 11 die CE-Kennzeichnung tragen dürfen, es sei denn, dass diese Prüfungen eine andere Zweckbestimmung der Produkte zum Gegenstand haben als die in dem Verfahren zur Bewertung der Konformität vorgesehenen. Die einschlägigen Bestimmungen des Anhangs X bleiben anwendbar.
Anhang III:
– Nr. 2.2. Erklärung zu den Medizinprodukten, die für klinische Prüfungen im Sinne von Anhang X bestimmt sind
– Nr. 3.2. Dokumentation zu den klinisch zu prüfenden Medizinprodukten
– Nr. 4. Aufbewahrungsfrist von Unterlagen
Anhang X:
– Nr. 2 Anforderungen an die Durchführung von klinischen Prüfungen
§§20 – 24 MPG
§ 20 Allgemeine Voraussetzungen zur klinischen Prüfung
§ 21 Besondere Voraussetzungen zur klinischen Prüfung
§ 22 Verfahren bei der Ethik-Kommission
§ 22a Genehmigungsverfahren bei der Bundesoberbehörde
§ 22b Rücknahme, Widerruf und Ruhen der Genehmigung oder Zustimmung
§ 22c Änderung der Genehmigung von klinischen Prüfungen
§ 23 Durchführung der klinischen Prüfung
§ 23a Meldung über Beendigung oder Abbruch von klinischen Prüfungen
§ 23b Ausnahmen zur klinischen Prüfung
§ 24 Leistungsbewertungsprüfung
Über die Verordnung über die klinische Prüfung von Medizinprodukten (MPKPV) werden zusätzlich noch die relevanten Gesichtspunkte für das Genehmigungsverfahren bei der Behörde, das Verfahren bei der Ethikkommission und die Durchführung der klinischen Prüfung für alle Beteiligten konkretisiert.
Ergänzt wird dies durch die Medizinprodukte-Sicherheitsplanverordnung (MPSV), in die zum Schutz der Patienten der Begriff des schwerwiegenden unerwünschten Ereignisses aufgenommen wurde. Durch die Verordnung über das datenbankgeschützte Informationssystem über Medizinprodukte (DIMDIV) wird das zentrale elektronische Einreichungsverfahren für die erforderlichen Anträge bei den Behörden und Ethikkommissionen für klinische Prüfungen mit Medizinprodukten geregelt.
Die Norm über die Klinische Prüfung von Medizinprodukten an Menschen – Gute klinische Praxis (DIN EN ISO 14155, 2012) legt die formellen Anforderungen an die gute klinische Praxis für die Durchführung der klinischen Prüfung mit Medizinprodukten fest, um die Sicherheit und Leistungsfähigkeit zu gewährleisten. Sie gibt eine detaillierte Anleitung zu den wichtigsten Abläufen der klinischen Prüfung, beschreibt die Studiendokumente und die Aufgaben von Sponsor und Prüfer.
Des Weiteren muss jede klinische Prüfung mit einem Medizinprodukt, analog zur Arzneimittelprüfung, im Einklang mit der Deklaration von Helsinki (in der letzten vom Weltärztekongress geänderten Fassung) stehen, zum Schutz der an einer klinischen Prüfung teilnehmenden Personen.
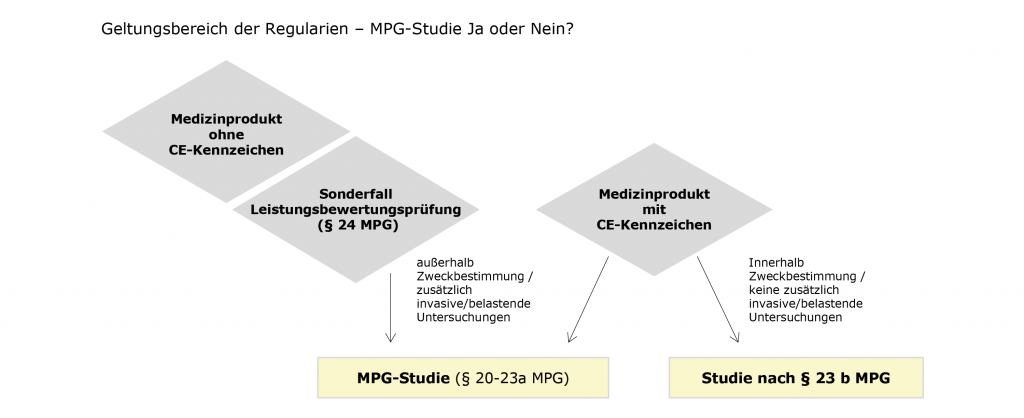
Ob es sich um eine klinische Prüfung nach § 20-23a MPG handelt und die unter Punkt 2 genannten Regularien/Vorschriften für die klinische Prüfung bei Medizinprodukten gelten, hängt im Wesentlichen von der Art der klinischen Prüfung ab.
Sie gelten für:
- Prüfungen mit Medizinprodukten (§ 1 MPKPV):
1. ohne CE-Kennzeichnung, deren Ergebnisse verwendet werden sollen um im Rahmen der Konformitätsbewertung ein CE-Kennzeichen zu erlangen.
2. mit CE-Kennzeichen,
2.1. deren Ergebnisse verwendet werden sollen um im Rahmen der Konformitätsbewertung eine neue Zweckbestimmung zu erlangen.
2.2. deren Ergebnisse Informationen zur klinischen Sicherheit und Leistung des Medizinprodukts liefern, sofern zusätzlich invasive oder andere belastende Untersuchungen durchgeführt werden.
- Leistungsbewertungsprüfungen von in-vitro Diagnostika (§24 MPG), bei denen:
1. invasive Probennahme ausschließlich oder in erheblich zusätzlicher Menge erfolgt.
2. zusätzlich invasive oder andere belastende Untersuchungen durchgeführt werden.
3. Ergebnisse für die Diagnostik verwendet werden sollen, ohne mit etablierten Verfahren bestätigt zu sein.
Sie gelten nicht für:
- Prüfungen mit CE-gekennzeichneten Medizinprodukten gemäß § 23b, wenn
1. die Medizinprodukte innerhalb der Zweckbestimmung angewendet werden.
2. keine zusätzlichen invasiven oder belastenden Untersuchungen durchgeführt werden./br> - Leistungsbewertungsprüfungen von in-vitro Diagnostika gemäß § 1 Abs. 2 MPKPV, bei denen eine nicht chirurgisch-invasive Probennahme ausschließlich oder in erheblicher zusätzlicher Menge aus der Mundhöhle erfolgt.
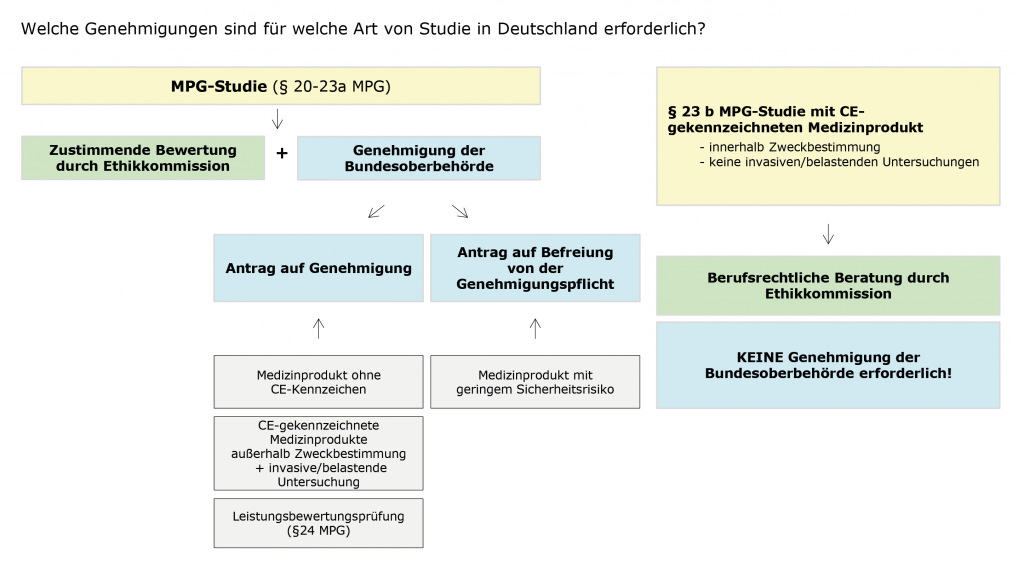
Welche Art von Genehmigung für eine klinische Prüfung erforderlich ist, hängt in erster Linie von der Art der Studie ab. Für alle klinischen Prüfungen die unter das MPG (§20-23a) fallen, ist das Vorliegen einer Genehmigung durch die Bundesoberbehörde und die zustimmende Bewertung durch die Ethikkommission erforderlich, erst dann darf mit der klinischen Prüfung begonnen werden.
Das Antragsverfahren bei der Bundesoberbehörde und der Ethikkommission sind in den §§ 3-8 MPKPV geregelt. Bei MPG-Studien muss man hinsichtlich des Genehmigungsverfahrens bei der Bundesoberbehörde noch unterscheiden zwischen einem:
- Antrag auf Genehmigung und
- Antrag auf Befreiung von der Genehmigungspflicht.
Antrag auf Genehmigung (gemäß § 3 MPKPV) ist bei der Bundesoberbehörde immer dann zu stellen, wenn es sich um eine MPG-Studie (§20-23a) handelt, die mit einem
- Medizinprodukt ohne CE-Kennzeichen durchgeführt wird.
- CE-gekennzeichneten Medizinprodukt durchgeführt wird, außerhalb der Zweckbestimmung und unter Einschluss zusätzlich invasiver und belastender Untersuchungen.
Antrag auf Befreiung von der Genehmigungspflicht (gemäß § 7 MPKPV) ist bei der Bundesoberbehörde immer dann zu stellen, wenn es sich um eine MPG-Studie (§20-23a) mit einem Medizinprodukt mit geringem Sicherheitsrisiko handelt.
Antrag auf zustimmende Bewertung durch die Ethikkommission ist unabhängig davon, ob man einen Antrag auf Genehmigung oder einen Antrag auf Befreiung von der Genehmigungspflicht bei der Bundesoberbehörde stellen muss, immer erforderlich.
Für alle anderen Arten von Studien die sogenannten §23b –Studien bezeichnet werden, ist keine Genehmigung durch die Bundesoberbehörde und kein Ethikvotum erforderlich. Für die an solchen Studien teilnehmenden Ärzte gelten die berufsrechtlichen Vorgaben, wonach eine entsprechende Ethikkommission zur Beratung mit einzubeziehen ist (§ 15 BO Ärzte).
Bei einer klinischen Prüfung mit einem Medizinprodukt mit geringem Sicherheitsrisiko kann die Bundesoberbehörde von einer Genehmigung absehen. Dazu muss ein entsprechender Antrag bei der Bundesoberbehörde gestellt werden.
Der Antrag auf Befreiung von der Genehmigungspflicht ist immer dann möglich, wenn folgende Voraussetzungen für die klinische Prüfung gegeben sind:
- Medizinprodukt der Klasse I,
- Nicht-invasives Medizinprodukt der Klasse IIa,
- CE-gekennzeichnetes Medizinprodukt, innerhalb der Zweckbestimmung und zusätzliche invasive oder belastende Untersuchungen,
- In-vitro Diagnostikum, das für die Leistungsbewertungsprüfung nach §24 bestimmt ist und
a. invasive Probennahme ausschließlich oder in erheblich zusätzlicher Menge erfolgt.
b. zusätzlich invasive oder andere belastende Untersuchungen durchgeführt werden.
Get the latest articles as soon as they are published: for practitioners in clinical research
Read about ideas & tools for effective clinical research
Follow today’s topics in clinical research
Knowledge base: study design, study management, digitalization & data management, biostatistics, safety
It’s free! Sign up now!